编辑丨&
细菌广泛存在于我们周围的环境中,它们生存与进化的方式和速度经常挑战人类的想象。即使是现在,有关微生物的各个方面仍存在不少未解之谜。
在细菌的高速进化中,除了基因突变,还有一种更高效的方式:基因水平转移(horizontal gene transfer),让耐药性、毒力等关键特征能在不同细菌之间迅速扩散。这背后的一类分子就是噬菌体诱导染色体岛(phage-inducible chromosomal islands, PICIs)。
而有这么一类更神秘:能形成衣壳的 cf-PICIs。科学家发现它们竟能跨物种传播,但具体机制一直没搞明白。直到帝国理工学院与 Google Research 联合提出一个新问题:能不能让 AI 来帮我们提出假设?
相关的研究成果以「AI mirrors experimental science to uncover a mechanism of gene transfer crucial to bacterial evolution」为题,于 2025 年 9 月 9 日发布在《Cell》。

论文链接:https://www.cell.com/cell/fulltext/S0092-8674(25)00973-0
AI co-scientist
为探索 AI 在构思具有创造性、新颖性与影响力的假设方面的潜力,研究团队测试了一种名为 AI co-scientist 的新型系统,研究对象则是上文中提到过的 cf-PICIs,一种能自己形成衣壳的噬菌体卫星病毒。它们被发现可以跨物种传播,但机制一直未明。
在过去的几年里,相关实验室一直致力于破解这其中的秘密,并在不久前拼凑出了解决方案。凭借这一知识,并确信科学界尚未意识到这一突破,该团队向 AI co-scientist 提出了一个假设:相同的 cf-PICIs 如何在不同的细菌物种中存在。
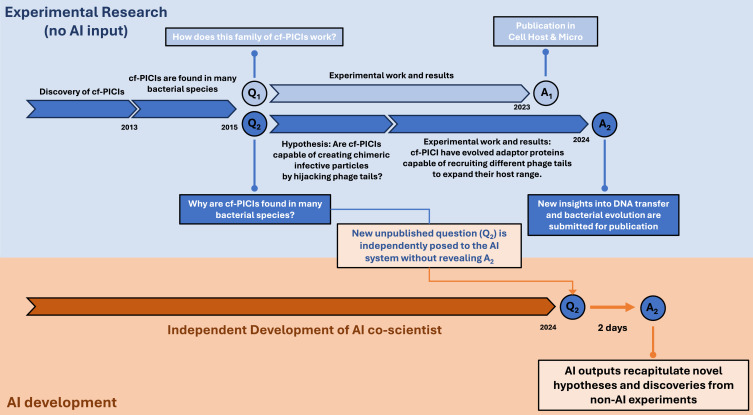
图示:AI 是如何发现基因转移机制的。
考虑到该系统并未专门接受噬菌体或卫星生物学或细菌进化方面的训练,团队假设这将提供一个无偏见的测试其生成强大假设的能力。不过结果显然出乎了他们的预料。
AI 的首个回答就击中了要害:它提出 cf-PICIs 的跨物种传播依赖于衣壳与噬菌体尾部的模块化组合。也就是说,cf-PICIs 自己能形成衣壳,但尾部必须借助不同噬菌体的「配件」,才能感染新宿主。
包括这个回答与其余的四个回答,AI 以优先级和可能性为其排序,并使用基于 Elo 评分的锦标赛框架对假设进行排名。它们分别为:
1.衣壳-尾相互作用:cf-PICIs 衣壳与广泛辅助噬菌体尾部的相互作用;
2.整合机制:cf-PICIs 如何整合到不同细菌物种的基因组中;
3.进入机制:cf-PICIs 除传统噬菌体受体识别之外的替代进入机制;
4.辅助噬菌体和环境因素:研究辅助噬菌体和更广泛的生态因素在 cf-PICIs 转移中的作用;
5.替代转移和稳定机制:其他可能有助于 cf-PICIs 拓宽宿主范围的转移机制,如接合、细胞外囊泡(EVs)和独特的稳定策略。
相比之下,研究团队让其他大模型也试了一遍:GPT、Claude、Gemini、DeepSeek……结果都没有提出正确的机制。只有 AI co-scientist 正中靶心。
假设的发现与验证
衣壳-尾相互作用被评为最有希望的假设,在该研究中,团队展示了 cf-PICIs 形成了一个新的生物实体,由 cf-PICI 基因编码的衣壳包装的 cf-PICI DNA 组成。这些衣壳没有尾巴,无法传播到新的细菌宿主。
由于噬菌体和卫星的宿主范围由它们的尾巴决定,尾巴与细菌表面结构结合,因此这种机制解释了为什么相同的 cf-PICIs 出现在不同的物种中。根据使用的尾巴不同,cf-PICI DNA 被传递到不同的宿主。
后续的实验进一步证明:些无尾的 cf-PICIs 病毒衣壳可以与感染不同物种的噬菌体的多个尾结合,这种能力是由适配器和连接器这两个 cf-PICIs 编码的蛋白质介导。通过在两个 cf-PICIs 之间交换这些蛋白质,团队证明了它们的表达决定了尾结合特异性,从而决定了宿主范围。
而 AI co-scientist 关于研究衣壳-尾相互作用的建议极具洞察力,在其合理且之前未被探索的想法中,研究团队认为,其所提出的,对囊膜和尾部的保守区域与适配蛋白表征方面的研究非常有针对性。
团队表示,如果能早些获取这些想法,研究的进程也许早就不会是现在这样。
图表:不同 AI 系统的比较。
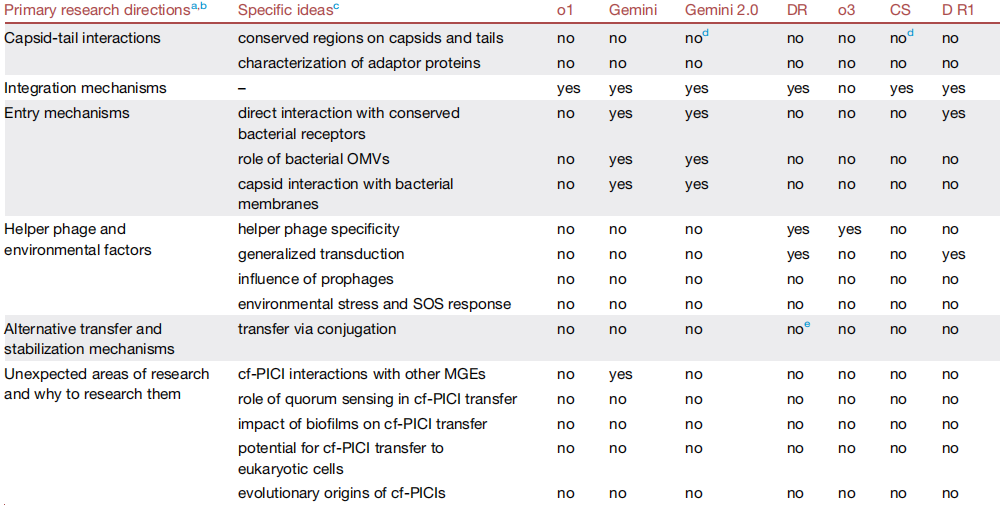
AI co-scientist 的假设反映了团队所走过的实验路径,却排除了由人类主观意识与偏见所带来的障碍。在团队为它设计的验证中,他们确实观察到 cf-PICIs 能与不同噬菌体的尾部模块结合,在剥夺尾部的情况下,cf-PICIs 的跨物种传播能力就消失了。
这印证了 AI 提出的机制,也为理解细菌如何快速传播耐药性提供了直接证据。
AI 与科学家的新关系
AI 在增强生物研究全科学流程方面展现出革命性的潜力,本次实验仅仅是提供了一个具体例子,说明了此类系统如何有助于假设生成和实验规划。
研究员自己也强调:AI 并不是替代,而是补充。它能帮人类更快缩小可能性范围,把宝贵的实验资源投向最值得验证的方向。像 cf-PICIs 这样的分子机制,如果能更早揭示,就能帮助研究者更好预测并控制耐药基因的扩散。