编辑丨&
随着科研人员对生物系统的理解达到单细胞和高空间分辨率,药理学方法也必须跟上,以匹配这种精确度,理解药物作用。
目前,常用的临床检测只能显示药物在某个器官里大致浓度,但无法看清药物真正结合在哪些细胞上。打个比方来说,药物在体内的去向常像被雾霾遮住的景象——一切都处在模糊的感知中,想要精确定位并不简单。
这种处在黑箱之中的现状被终结了。以美国斯克里普斯研究中心(Scripps Research)与霍华德·休斯医学研究所(Howard Hughes Medical Institute)为主的研究团队开发了一种突破性的成像技术,能够照亮整个小鼠体内药物结合的单个细胞。
相关研究内容以「Mapping cellular targets of covalent cancer drugs in the entire mammalian body」为题,于 2025 年 12 月 22 日发布在《Cell》。

论文链接:https://www.cell.com/cell/fulltext/S0092-8674(25)01365-0
vCATCH
体积清除辅助组织点击化学(volumetric clearing-assisted tissue click chemistry),后称为 vCATCH,是该团队所开发的能够在体内精确定位药物、细胞结合情况的成像技术。
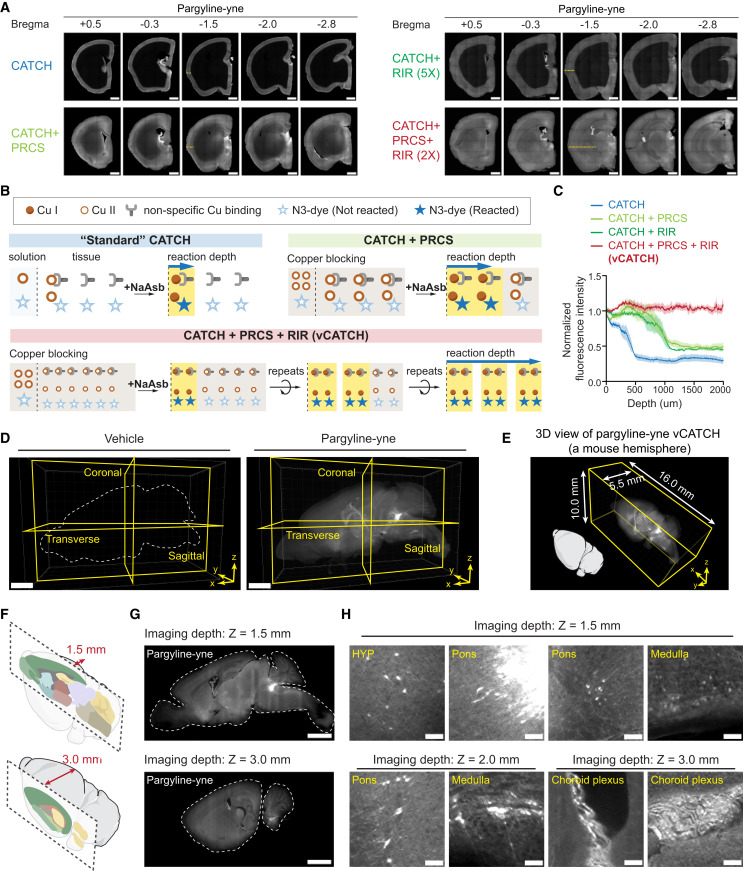
图示:建立深层组织点击反应的原理。
vCATCH 是对 2022 年提出的 CATCH 方法的升级方向,主要采用以下几种关键技术的组合:
体内部位标记药物分子:将包含可与目标蛋白发生共价作用的过量的铜进行适当的化学改造,以深入染色器官。
体内给药与固定:药物按常规方式给药后,在体内与目标结合。随后对整个动物组织进行取样与预处理。
「Click Chemistry」反应标记结合位点:使用高选择性的化学反应给结合了药物的细胞分子进行荧光标记。该反应极具专一性并能穿透深层组织。
体内组织清晰化 + 三维成像:通过组织清晰化方法让整个组织透明,并使用光片荧光显微成像系统获全身三维数据。
AI 辅助图像分析:成像产生的数据通常以「TB 级」规模呈现,使用先进的 AI 数据管线自动识别并定位每一个结合细胞。
测试与结果
为了测试这一新方法,叶的实验室绘制了两种靶向癌症药物的结合:用于治疗血癌的 Ibrutinib(Imbruvica)和用于非小细胞肺癌处方的 Afatinib(Gilotrif)。
对于前者,vCATCH 分辨出的结合定位显示不仅在血液细胞中,还在心脏、血管壁甚至肝脏的免疫细胞中出现明确结合信号,这一发现可能解释其临床上观察到的心血管副作用。
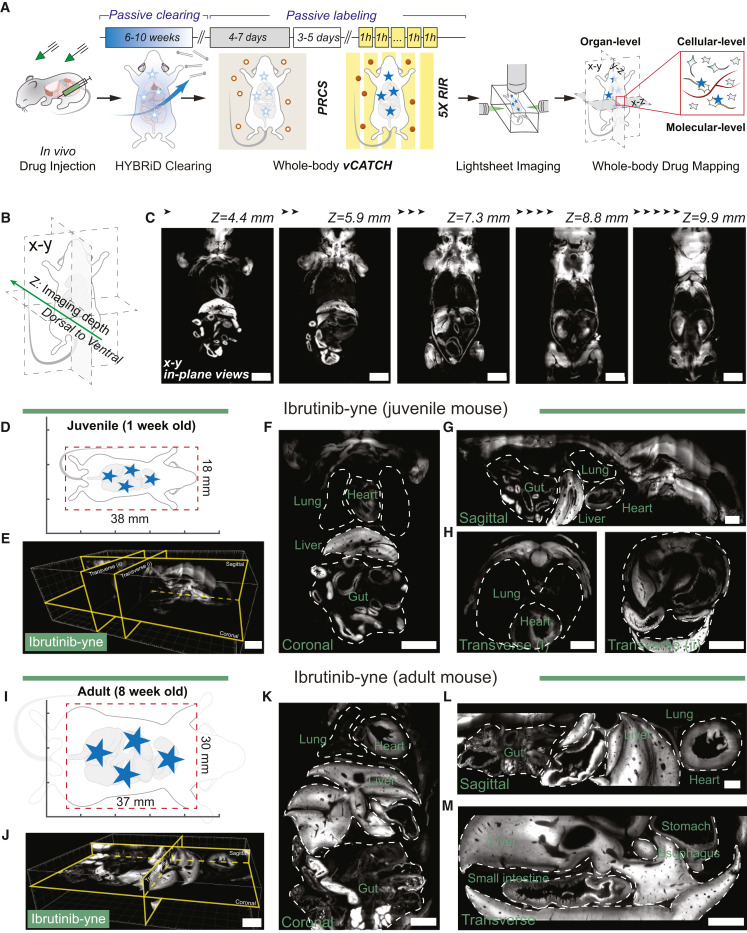
图示:vCATCH 显示了全体 TKI 分布,具有高空间分辨率。
而对于后者,表现出了如预期结果中的一致性。
除此之外,团队还发现:尽管这两种药物都与肾脏结合,但它们在器官内表现出不同的模式。更高分辨率的 vCATCH 显示了它们在器官内分布上的差异:Afatinib 在肝组织中表现出冠状信号,而 Ibrutinib 则与稀疏散布的单个细胞相关,这一点由光片和共焦成像均有体现。
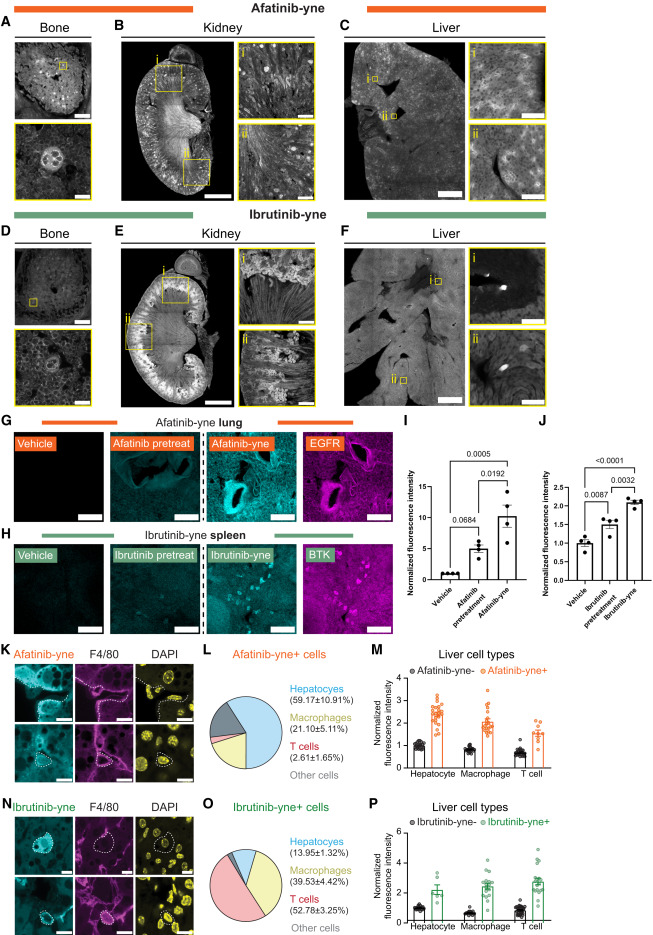
图示:药物富集组织中 TKI 参与的细胞类型特征。
药物开发的全新视角
传统药效评估局限于整体组织层级,而 vCATCH 提供了 逐细胞的药物结合情况,有助于识别药物靶标之外的非预期结合位点,这正是许多未知副作用的根源。
在药物开发的早期阶段,研发团队可以凭此快速观察到药物与细胞的交互,也可以从 vCATCH 处获得有关副作用的细胞级别解释。结合 AI 工具分析全身结合数据后,甚至可以对不同小鼠个体乃至未来人体样本执行比对分析,在个性化医学中具备潜在应用。
相关报道:https://www.eurekalert.org/news-releases/1110881